Amoniac là một trong những hóa chất phổ biến quan trọng trong nền công nghiệp hóa chất. Vậy amoniac là chất gì? Chắc các bạn cũng biết amoniac luôn có trong nhà vệ sinh và ngửi được mùi khai đặc trưng của nó. Tuy nhiên khi hít phải amoniac có nồng độ cao sẽ làm ảnh hưởng nghiêm trọng đến sức khỏe. Hãy tìm hiểu amoniac là chất gì qua bài viết dưới đây của Gockhampha.edu.vn.COM.VN nhé!
Bạn đang đọc: Amoniac là chất gì? Cấu tạo phân tử, Điều chế và Ứng dụng của amoniac
Contents
Amoniac là chất gì và Cấu tạo phân tử amoniac
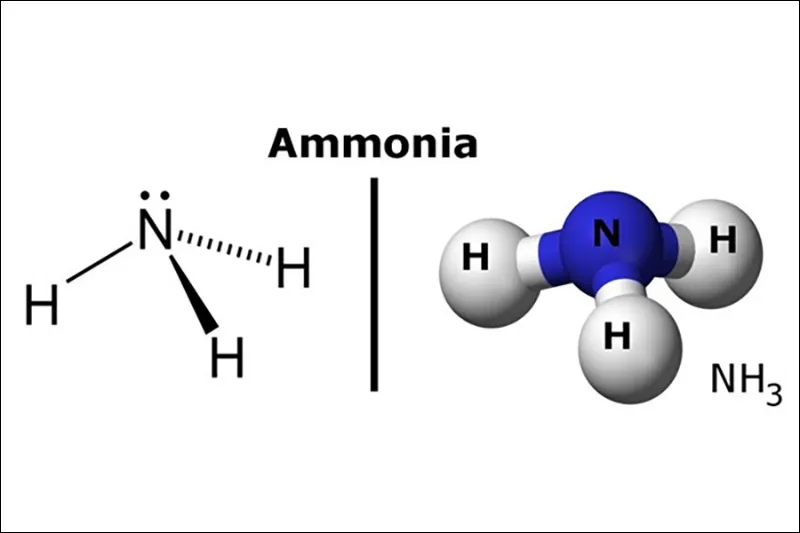
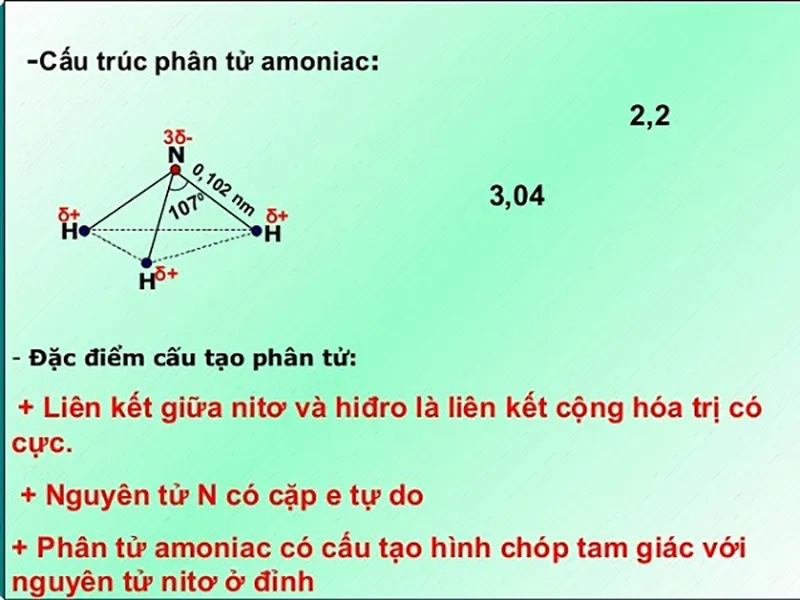
Phân tử (NH_{3}) có cấu tạo hình chóp, với nguyên tử nitơ ở đỉnh liên kết cộng hóa trị với 3 nguyên tử hidro ở đáy tam giác. Do nitơ có ba electron độc thân nên có thể tạo 3 liên kết cộng hóa trị trên với hidro.
Tính chất vật lý amoniac
Amoniac là một chất khí không màu, có mùi khai và nhẹ hơn không khí.
Khí (NH_{3}) tan rất nhiều trong nước: 1l nước ở 80 độ C có thể hòa tan 800l khí (NH_{3}). Amoniac là chất tan trong nước tạo thành dung dịch amoniac. Dung dịch amoniac đậm đặc có nồng độ 25%.
Tính chất hóa học amoniac
Tính bazo yếu
-
Tác dụng với nước
Khi tan trong nước, một phần nhỏ phân tử amoniac kết hợp với ion (H^{+}) trong nước theo phương trình:
(NH_{3} + H_{2}O rightleftharpoons NH_{4}^{+} + OH^{-})
Chính (OH^{-}) làm cho dd có tính bazo, làm phenolphtalein chuyển từ không màu sang màu hồng, quỳ tím chuyển sang màu xanh. Tuy nhiên trong dd, amoniac là một bazo yếu.
-
Tác dụng với axit
(2NH_{3} + H_{2}SO_{4}rightarrow (NH_{4})_{2}SO_{4})
Khi đặt hai bình dd HCl đặc và (NH_{3}) đặc đều mở nút thì sẽ tạo thành khói trắng là tinh thể muối amoni clorua theo phương trình:
(NH_{3}_{(k)} + HCl_{(k)}rightarrow NH_{4}Cl_{(r)})
Phản ứng đặc trưng này dùng để nhận ra khí amoniac.
-
Tác dụng với dung dịch muối
Dung dịch amoniac có khả năng làm kết tủa nhiều hidroxit kim loại:
(Al^{3+} + 3NH_{3} + 3H_{2}Orightarrow Al(OH)_{3} + 3NH_{4}^{+})
Khả năng tạo phức của amoniac
Dung dịch amoniac có khả năng hòa tan hidroxit hay muối ít tan của một số kim loại, tạo thành các dung dịch phức chất.
Thí dụ:
(Cu(OH)_{2} + 4NH_{3}rightarrow [Cu(NH_{3})_{4}](OH)_{2})
(Cu(OH)_{2} + 4NH_{3}rightarrow [Cu(NH_{3})_{4}]^{2+} + 2OH^{-})
Xanh thẫm
(AgCl + 2NH_{3}rightarrow [Ag(NH_{3})_{2}]^{+} + Cl^{-})
Tính khử của amoniac
-
Tác dụng với oxi
Amoniac cháy trong khí với ngọn lửa màu vàng:
(4NH_{3} + 3O_{2}overset{t^{0}}{rightarrow}2N_{2} + 6H_{2}O)
Khi có xúc tác: (4NH_{3} + 3O_{2}xrightarrow[t^{0}]{xt} 4NO + 6H_{2}O)
-
Tác dụng với clo
Dẫn khí (NH_{3}) vào bình chứa khí clo, (NH_{3}) bốc cháy tạo ngọn lửa có khói trắng.
(2NH_{3} + 3Cl_{2}rightarrow N_{2} +6HCl)
Khói trắng do HCl vừa tạo thành hóa hợp với (NH_{3}) tạo (NH_{4}Cl)
-
Tác dụng với oxit kim loại
(2NH_{3} + 3CuOoverset{t^{0}}{rightarrow}3Cu + N_{2} +3H_{2}O)
Tìm hiểu thêm: Các dạng bài tập este trong đề thi đại học và phương pháp giải
Điều chế amoniac
Trong phòng thí nghiệm
(2NH_{4}Cl + Ca(OH)_{2}overset{t^{0}}{rightarrow}2NH_{3} + CaCl_{2} + 2H_{2}O)
Để làm khô khí dẫn khí qua bình đựng vôi sống CaO
Trong công nghiệp
(N_{2}_{(k)} + 3H_{2}_{(k)}rightleftharpoons 2NH_{3}_{(k)})
Ứng dụng của amoniac
Amoniac thường có trong nước tiểu, sinh ra trong quá trình bài tiết và thối rữa xác sinh vật. Amoniac được dùng để điều chế phân đạm, điều chế axit nitric, là chất sinh hàn, sản xuất hiđrazin (N_{2}H_{4}) dùng làm nhiên liệu cho tên lửa. Bên cạnh đó, dung dịch amoniac còn được dùng làm chất tẩy rửa.

>>>>>Xem thêm: Điều chế axetilen trong phòng thí nghiệm và Ứng dụng của axetilen
Tác hại của amoniac với sức khỏe con người
Tác hại của amoniac
Khí amoniac với nồng độ đậm đặc rất nguy hiểm đối với sức khỏe con người. Cụ thể:
- Hít phải: gây bỏng niêm mạc mũi, cổ họng và đường hô hấp. Điều này làm phá hủy đường thở dẫn đến suy hô hấp. Vì amoniac có tính ăn mòn.
- Tiếp xúc trực tiếp: da, mắt, họng, phổi có thể bị bỏng rất nặng. Những vết bỏng có thể gây mù vĩnh viễn, bệnh phổi, hoặc tử vong.
- Nuốt phải: Vô tình nuốt phải amoniac đậm đặc có thể bỏng ở miệng, cổ họng và dạ dày, đau dạ dày nghiêm trọng, gây nôn.
Xử lý khi ngộ độc amoniac
Amoniac nồng độ cao rất độc với con người tuy nhiên không phải ai cũng biết cách xử lý khi tiếp xúc và bị ngộ độc khí amoniac. Dưới đây là những cách sơ cứu khi bị ngộ độc amoniac:
- Khi hít phải khí amoniac nhanh chóng di chuyển nạn nhân đến nơi thoáng khí, cởi sạch quần áo dính amoniac.
- Súc sạch miệng với nước sạch trong trường hợp nuốt phải amoniac. Cho nạn nhân uống 1-2 cốc sữa.
- Tiếp xúc với dd amoniac thì rửa sạch amoniac dính trên da với xà phòng và nước, rửa mắt sạch với nhiều nước.
- Sau cùng là đưa nạn đến trạm y tế hoặc bệnh viện để cứu chữa.
Hy vọng qua bài viết bạn đã biết được amoniac là chất gì? Amoniac được sử dụng phổ biến trong công nghiệp nhưng nó cũng gây hại đối với con người. Hãy nắm rõ cách sơ cứu khi bị ngộ độc amoniac đậm đặc để cứu chữa kịp thời cho bản thân và mọi người xung quanh nhé. Nếu có thắc mắc gì về bài viết “amoniac là chất gì” hãy để lại câu hỏi bên dưới để chúng mình cùng thảo luận nhé!