Khí CO2 còn được gọi là cacbon đioxit và đóng vai trò quan trọng trong ngành công nghiệp thực phẩm, khai thác khoáng sản cũng như trong đời sống thường ngày. Vậy khí CO2 là gì và khí CO2 có độc không? Cùng Gockhampha.edu.vn.COM.VN tìm hiểu ngay trong bài viết này nhé!
Bạn đang đọc: Khí CO2 là gì? Tính chất, nguồn gốc và ứng dụng Cacbon dioxit
Contents
CO2 là gì? Cấu tạo phân tử
CO2 là gì?
Cacbon đioxit là một hợp chất khá quen thuộc và được gọi với nhiều tên gọi khác nhau như thán khí, anhiđrít cacbonic hoặc khí cacbonic. Về công thức hóa học, Cacbon đioxit được ký hiệu là CO2. Về cấu tạo, hợp chất CO2 được cấu thành từ 1 nguyên tử cacbon và 2 nguyên tử oxy.
CO2 có thể tồn tại ở nhiều môi trường vật lý khác nhau và ở mỗi môi trường, hợp chất này sẽ tồn tại ở các dạng khác nhau. Ví dụ như trong điều kiện nhiệt độ bình thường, CO2 sẽ tồn tại dưới dạng thể khí và có nồng độ khá thấp trong bầu khí quyển của Trái Đất. Trong khi đó dạng rắn, CO2 sẽ được gọi là băng khô.

Cấu tạo phân tử CO2
Cấu tạo của CO2 bao gồm 1 nguyên tử cacbon và 2 nguyên tử oxy. Trong cấu trúc của phân tử này, Cacbon sẽ nằm ở giữa, 2 nguyên tử oxy sẽ nằm ở 2 bên và mỗi nguyên tử cacbon sẽ liên kết với oxy bằng các liên kết ba bởi sự chia sẻ cặp electron giữa các nguyên tử này với nhau.

Các tính chất của CO2
Tính chất hóa học của CO2
CO2 có tính chất hóa học tiêu biểu của một oxit axit.
- CO2 có khả năng tan trong nước và tạo thành axit cacbonic (một axit yếu):
CO2 + H2O ⇌ H2CO3
- Ngoài ra, CO2 cũng có thể tác dụng với các oxit bazơ, gây ra các phản ứng tạo ra muối:
CaO + CO2 → CaCO3 (phản ứng tạo ra muối canxi cacbonat)
- CO2 cũng có thể tác dụng với dung dịch bazơ, tạo thành các muối và nước:
NaOH + CO2 → NaHCO3 (muối bicarbonat natri và nước)
2NaOH + CO2 → Na2CO3 + H2O (muối cacbonat natri và nước)
CO2 bền, ở nhiệt độ cao bị nhiệt phân một phần và tác dụng được với các chất khử mạnh
CO2 + 2Mg → 2MgO + C
CO2 + C → 2CO
Lưu ý: CO2 không được dùng để dập tắt các đám cháy kim loại.
CO2 còn được dùng để sản xuất ure
CO2 được sử dụng để sản xuất urea (công thức hóa học: (NH2)2CO) thông qua hai bước phản ứng:
Bước 1: CO2 tác dụng với hai phân tử amoniac (NH3) để tạo ra amoni cacbonat:
CO2 + 2NH3 → NH4OCO-NH2 (amoni cacbonat)
Bước 2:Tiếp theo, amoni cacbonat phân hủy ở nhiệt độ cao (khoảng 1800°C) và áp suất 200 atm để tạo ra nước (H2O) và urea ((NH2)2CO):
NH4OCO-NH2 → H2O + (NH2)2CO (ở điều kiện cao nhiệt; 200 atm

Tính chất vật lý của CO2
CO2 là một chất khí không màu, không mùi và có vị chua nhẹ ở điều kiện bình thường. Đồng thời CO2 cũng có thể hòa tan được trong nước. So với không khí, CO2 nặng hơn gấp 1,524 lần.
Khí CO2 không tham gia vào các phản ứng cháy và ở nhiệt độ khoảng -78 độ C, CO2 sẽ bị chuyển từ thể khí sang thể lỏng. Không chỉ vậy, ở nhiệt độ cao khoảng 2000 độ C, CO2 sẽ bị phân hủy và tạo ra CO, O2.

Khí CO2 sinh ra từ đâu
- Quá trình hô hấp của người và động vật
C6H12O6 + 6O2 → 6CO2 + 6H2O
- Quá trình lên men bia rượu
C6H12O6 → 2CO2 + 2C2H5OH
- Quá trình đốt cháy nhiên liệu
CxHy + (x + y/4)O2 → xCO2 + y/2H2O
- Trong công nghiệp
C + O2 → CO2 (đốt cháy hoàn toàn than cốc trong không khí)
CaCO3 → CaO + CO2 (ở 1000°C)
- Trong phòng thí nghiệm:
CaCO3 + 2HCl → CaCl2 + CO2 + H2O

Ứng dụng của CO2
Trong công nghệ thực phẩm
- Một trong những ứng dụng quan trọng nhất của CO2 đó là làm lạnh, giúp lưu trữ và vận chuyển các thực phẩm đông lạnh dễ dàng hơn.
- CO2 cũng được dùng để tạo khí trong các sản phẩm thức uống có ga như: Coca, Pepsi, 7up,… Không chỉ vậy, CO2 còn đóng vai trò lớn trong việc điều hòa nước uống.
- Bột nở được sử dụng khá phổ biến trong chế biến nấu ăn, đặc biệt là làm bánh. Môt thành phần không thể thiếu trong bột nở đó là CO2, loại khí này đóng vai trò chính trong việc làm phồng bột, tạo lỗ chứa bọt khí, nhờ vậy mà bánh sẽ trở nên mềm mịn hơn.
- CO2 siêu lưỡng tính hay còn được gọi là Supercritical carbon dioxide đóng vai trò chính trong việc chiết xuất màu sách và hương vị từ các loại thực phẩm. CO2 còn giúp loại bỏ dầu mỡ và tạo ra các loại thực phẩm an toàn, ít béo, tinh khiết.
Tìm hiểu thêm: Xicloankan là gì? Cấu tạo, tính chất và cách điều chế của Xicloankan

Trong công nghiệp
- Trong áo phao cứu hộ thường có chứa các hộp nhỏ chứa CO2 đã nén, nhờ vậy mà áo phao có thể nổi lên dễ dàng trên mặt nước.
- Ngoài ra, các ống thép có chứa khí cacbonic nén thường được bán ra thị trường để phục vụ cho các sản phẩm khác như súng hơi, máy phun sơn, bơm lốp xe,…
- Carbon dioxide siêu lưỡng tính được sử dụng như một chất pha lỏng trong quá trình phun sơn, làm giảm 80% dung môi hữu cơ và nhờ vậy mà làm giảm thiểu được nhiều vấn đề gây ảnh hưởng xấu đến môi trường.
- Với tốc độ bốc hơi nhanh, khí CO2 thường được ứng dụng trong ngày công nghiệp khai thác than để tạo nên các vụ nổ trong mỏ.
- CO2 là một tác nhân nén và giúp làm giảm độ nhớt của dầu thô khi hòa tan dầu trong lòng đất, từ đó dầu sẽ chảy nhanh hơn khi đưa vào giếng hút.
- Một trong những ứng dụng quan trọng của CO2 đó là sản xuất ure:
CO2 + 2NH3 → H2O + (NH2)2CO (ở nhiệt độ 1800°C và áp suất 200 atm)

Ứng dụng trong đời sống
- Trong các bình cứu hỏa thường chứa chủ yếu là CO2 lỏng và được nén lại để dập lựa.
- CO2 ở dạng rắn thường được gọi là băng khô và được ứng dụng trong việc làm sạch bề mặt thay cho cát, tạo mưa nhân tạo, khói trên sân khấu,…
- Khi kết hợp CO2 với oxy và một số loại khí khác có thể tạo thành hỗn hợp khí hô hấp, được sử dụng để kích thích quá trình hít thở nhanh và sâu. Hỗn hợp khí này còn hỗ trợ các vấn đề liên quan đến hệ hô hấp của con người.
- Thực vật trong tự nhiên dùng CO2 để quang hợp, cụ thể là chuyển đổi ánh sáng thành năng lượng hóa học.
- Để làm giàu bầu khí quyển trong các nhà kính khi nuôi trồng thực vật, ta có thể bổ sung CO2 nhằm thúc đẩy quá trình tăng trưởng của cây trồng, cải thiện hiệu suất trồng trọt.

Cách xử lý khi bị ngộ độc CO2
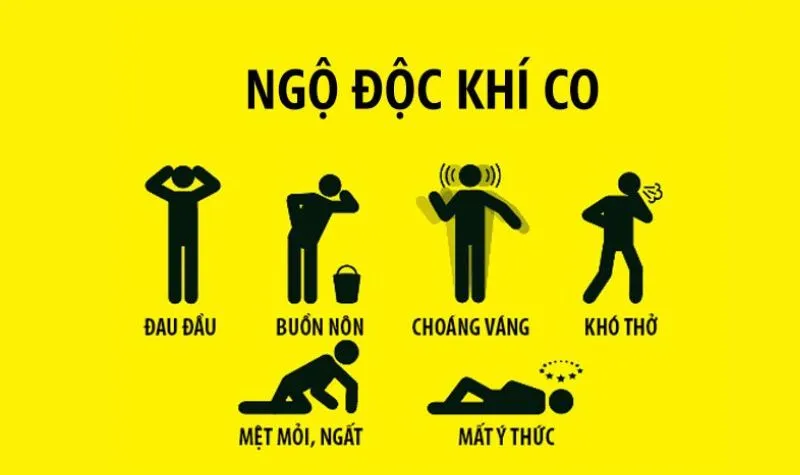
Các triệu chứng khi ngộ độc CO2
- Người bị ngộ độc khí CO2 có thể gặp phải các vấn đề như: Đau tức ngực, đau đầu, mệt mỏi, chóng mặt, buồn ngủ, buồn nôn và thậm chí là các cơn đau tức ngực đột ngột.
- Nếu tiếp xúc CO trong thời gian dài hoặc với nồng độ cao, các triệu chứng có thể nặng hơn như: Nôn mửa, nhầm lẫn, mất ý thức và suy nhược cơ.
- Các triệu chứng có mức độ nặng hay nhẹ là khác nhau ở mỗi người. Những đối tượng dễ bị ảnh hưởng nghiêm trọng khi bị ngộ độc là trẻ em, người cao tuổi, người mắc bệnh phổi hoặc bệnh tim, người có nồng độ CO trong máu cao (như người hút thuốc lá), phụ nữ mang thai và thai nhi.
Cách xử lý khi bị ngộ độc
- Với tính chất của CO2 là nặng hơn không khí 1,524 lần nên nạn nhân nên di chuyển đến những vị trí cao hơn sàn nhà, mặt đất để tránh tiếp xúc với khí CO2.
- Khi cảm thấy vấn đề ngộ độc ngày càng nghiêm trọng và nguy hiểm đến tính mạng, nạn nhân nên tìm cách để liên lạc với đội ngũ cấp cứu y tế để được hỗ trợ.
- Trong trường hợp không quá khẩn cấp, nạn nhân có thể liên lạc với trung tâm xử lý chống độc để được hướng dẫn khắc phục và hỗ trợ.
- Chỉ những người đã được đào tạo mới được sơ cứu bằng việc cấp oxy cho người bị ngộ độc CO2 để đảm bảo an toàn cho nạn nhân.
Lưu ý khi sử dụng và bảo quản CO2
- Van điều tiết khí của dụng cụ chứa khí CO2 nên được trang bị thêm một bộ phận sấy nhiệt để hạn chế tối đa tình trạng đóng băng và bịt kín đường cấp khí.
- Nên sử dụng mặt nạ thở có van để bảo vệ đường hô hấp của bạn khi gặp phải sự cố và hạn chế ngộ độc khí CO2.
- Lắp đặt thêm các thiết bị phát hiện khí để phòng tránh cũng như kịp thời xử lý khi sử dụng khí CO2.

>>>>>Xem thêm: Tìm hiểu chuyển đổi giữa khối lượng thể tích và lượng chất
Bài viết đã giúp bạn giải đáp thắc mắc khí CO2 là gì và những lưu ý quan trọng khi sử dụng khí CO2 để phòng tránh ngộ độc loại khí này. Chúc bạn có được những thông tin hữu ích để bảo vệ mình trong những trường hợp bị rò rỉ khí CO2 và hẹn gặp lại trong những bài viết tiếp theo của Gockhampha.edu.vn.COM.VN nhé!

